每隔两周,一位护士都会拜访住在科罗拉多州丹佛市的 43 岁马蒂·雷斯维格,并给他注射一种名为 gantenerumab 的实验性药物。每个月,雷斯维格都会开车进城进行脑部扫描,以确保该药物没有引起任何出血。每年,他都会飞往密苏里州圣路易斯市,进行为期四天的脑部扫描、脊髓穿刺、血液分析以及详尽的记忆力和推理能力测试。
雷斯维格身体健康,经营着两家当地企业。他经历这一切,是因为他有一种罕见的基因突变,几乎可以肯定他会患上早发性阿尔茨海默病。他希望他参与了九年的国际临床试验可能预防,或至少延缓症状的发作,否则这些症状将在几年内出现。
“我总是尽我所能为研究人员提供尽可能多的帮助——即使结果证明对我没有帮助,也可能会帮助我的孩子们,”他说。
关于支持科学新闻业
如果您喜欢这篇文章,请考虑通过以下方式支持我们屡获殊荣的新闻业 订阅。通过购买订阅,您正在帮助确保未来能够继续讲述关于塑造我们当今世界的发现和想法的有影响力的故事。
这项试验是试图了解在症状开始之前治疗阿尔茨海默病的根本原因是否可能是应对这种造成巨大损失的疾病的最佳方法之一。正在接受审查的药物都是抗体,这些抗体被开发出来用于靶向和清除大脑中的淀粉样蛋白 β 蛋白,这些蛋白会聚集在一起形成称为斑块的毒性团块(参见“抗淀粉样蛋白抗体”)。这些药物与 Biogen 公司在马萨诸塞州剑桥市生产的 aducanumab 属于同一类型,后者去年获得了美国食品和药物管理局 (FDA) 的临时批准,用于治疗轻度阿尔茨海默病,这在很大程度上归功于其去除淀粉样蛋白 β 的能力。
神经学家保罗·艾森说,由于这种毒性蛋白质是几种痴呆症的特征,这些抗体研究也可能为如何治疗全球 5500 万患有这些疾病的人提供线索。艾森是位于圣地亚哥的南加州大学的神经学家,也是美国阿尔茨海默病临床试验联盟的负责人。大多数痴呆症发生在 65 岁之后;所有这些都被证明是顽固不治的。在全球 100 多项试验中,大多数旨在治疗疾病的症状,而不是其根本原因。
但艾森预见到一个未来——也许就在十年左右之后——阿尔茨海默病的大部分负担实际上可能会被预防。“我们正朝着从中年开始对人们进行血液测试的方向发展,并用药物治疗那些显示出淀粉样蛋白异常的人,这些药物可以减少淀粉样蛋白斑块的生成,”他说。“我对此感到乐观。”
要使这种充满希望的观点成为现实,还需要很多事情步入正轨。大型临床试验必须证明这些疗法有效,并且必须证明清除淀粉样蛋白的药物是安全且负担得起的。在经历了数十年的挫折和失败的临床试验之后,一些痴呆症研究人员更倾向于表示谨慎。“该领域正在冒险进行可能耗资数十亿美元的研究,”明尼苏达州罗切斯特市梅奥诊所的神经学家大卫·克诺普曼说。
答案需要一段时间才能出现。一些阿尔茨海默病预防试验才刚刚开始,一些正在进行的试验可能会持续到下一个十年。
.jpeg?w=900)
阿尔茨海默病患者的大脑 PET(正电子发射断层扫描)显示淀粉样蛋白斑块的积聚(圈出),这在健康大脑中不存在。图片来源:Science History Images/Alamy Stock Photo
尽早介入
1986 年,英国诺丁汉的卡罗尔·詹宁斯写信给遗传学家约翰·哈迪,询问她是否可以在他的研究中发挥作用。就像雷斯维格一样,詹宁斯也有许多亲戚死于早发性痴呆症。哈迪的团队当时在伦敦大学学院,对阿尔茨海默病的遗传学很感兴趣,并邀请詹宁斯一家捐献血液给他们的项目。
几年后,该团队确定了受影响家庭成员共有的突变。它位于一个基因中,该基因编码一种位于神经元膜中的大型蛋白质,即淀粉样前体蛋白 (APP)。
大脑中的 APP 被一组酶切割成淀粉样蛋白 β 和其他短链淀粉样蛋白。在健康的大脑中,这些淀粉样蛋白肽可能具有有用的功能,但随着时间的推移,它们会积累——可能是因为大脑清除它们的分子系统效率降低——并聚集在一起形成斑块。在 APP 编码基因发生突变的人中,淀粉样蛋白 β 蛋白更具粘性或更丰富,并且疾病的发生早于没有该突变的人。
这是阿尔茨海默病淀粉样蛋白假说的基础,该假说由哈迪及其同事在发现致病性 APP 突变后首次提出。根据该理论,预防淀粉样蛋白 β 积累的触发事件可能会减缓疾病进程——甚至从一开始就阻止其发生。
制药和生物技术公司着手靶向淀粉样蛋白系统,开发阻止切割 APP 的酶的药物,或创建针对淀粉样蛋白 β 肽的抗体。但他们的药物在临床试验中不断失败。五项针对阻断淀粉样蛋白切割酶 β-分泌酶的药物的 III 期临床试验因副作用而中止,这些副作用使认知能力暂时恶化。另一种酶 γ-分泌酶的阻断剂也遭遇了同样的命运。一次又一次,旨在附着和结合淀粉样蛋白 β 的抗体试验未能改善人们的临床症状。至少有一家主要的制药公司辉瑞公司于 2018 年退出了阿尔茨海默病领域。
一连串的失败使研究界分裂成不同的阵营。一个阵营认为,如果靶向淀粉样蛋白不起作用,那么淀粉样蛋白假说一定是错误的。克诺普曼接受 APP 加工是疾病启动过程的一部分,但他说淀粉样蛋白 β 的作用尚未得到证实。“例如,其他 APP 切割产物可能对疾病过程更重要,”他说。
另一个阵营认为,试验设计不佳,特别是由于他们招募了已经开始表现出阿尔茨海默病早期迹象的人。
“事实是,为了优化去除淀粉样蛋白的潜在影响,你需要尽早这样做,”艾森说。淀粉样蛋白 β 的积累早在其损害足以引起症状的许多年前就开始了其缓慢而无声的破坏活动,他说。“阿尔茨海默病的总持续时间超过 25 年,而试验仅在神经退行性变不断恶化的最后十年进行。”
动物研究支持了这一见解。在基因改造为过度表达 APP 的小鼠中,在检测到淀粉样蛋白 β 沉积物之前用 aducanumab 治疗幼鼠,导致沉积物显着减少,并且六个月后大脑中疾病迹象减少。
当 FDA 去年 6 月做出有争议的决定批准 Biogen 的 aducanumab 时,它认识到了这种长期前景:该药物去除淀粉样蛋白 β 的能力使其有可能减少阿尔茨海默病的症状。Biogen 对患有轻度阿尔茨海默病的人进行的 aducanumab 大型安慰剂对照试验并未明确改善他们的临床症状,但该药物在清除他们大脑中的淀粉样蛋白斑块方面做得很好。该机构宣布 aducanumab 是第一个影响该疾病生物学原因的治疗方法。
该决定激怒了许多研究人员,他们声称 FDA 降低了其标准。(克诺普曼因此问题辞去了 FDA 咨询委员会的职务。)但在接下来的几个月中,来自其他药物试验的更多数据出现,显示随着淀粉样蛋白 β 的清除,认知能力下降的趋势略有减缓,以及阿尔茨海默病进展的其他生物标志物(例如称为 tau 蛋白的蛋白质的积累)的减少。当年晚些时候,该机构将另外三种抗体纳入快速通道审查程序:Genentech-Roche 的 gantenerumab、Biogen-Eisai 的 lecanemab 和 Eli Lilly 的 donanemab。与 aducanumab 类似,所有三种药物都在早期试验中被证明可以清除斑块。
“这些药物是重大的、重大的游戏规则改变者,”伦敦大学学院英国痴呆症研究所所长、神经科学家巴特·德·斯特鲁珀说。“它们将使淀粉样蛋白假说得到明确的检验。”
许多研究人员一致认为,检验该假说的最佳方法——也是阻止疾病发展的最佳方法——是尽早给人们服用这些药物,而无需等待阿尔茨海默病症状首先出现。
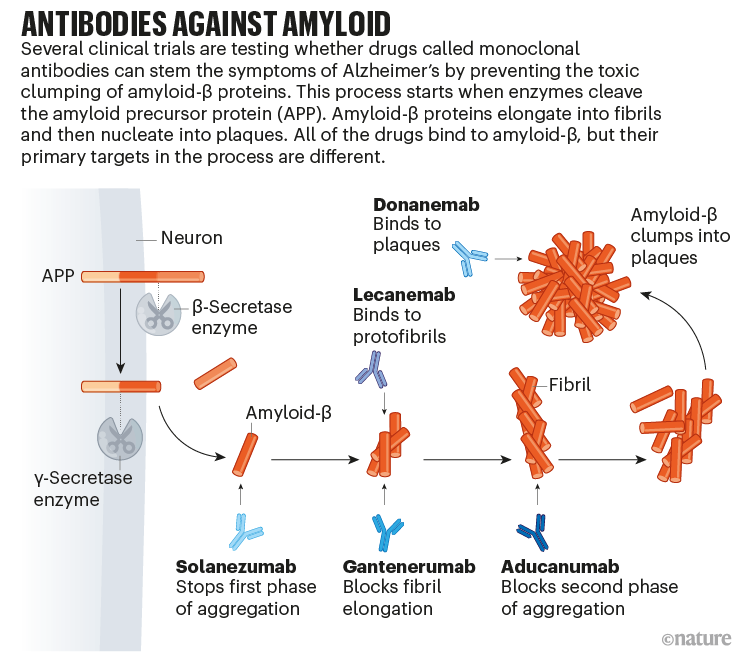
图片来源:Nik Spencer/《自然》
时机至关重要
哈迪认为,即使是最早的试验的设计者也可能意识到他们招募患者的时间太晚了。“通过回顾镜来看,这一点很清楚——数据已经存在,”他说。在 1980 年代,加利福尼亚大学圣地亚哥分校的病理学家乔治·格伦纳和他的同事发现,唐氏综合征患者相对年轻时就会患上痴呆症。他们认为,这是因为唐氏综合征患者多了一条 21 号染色体(APP 基因位于该染色体上)。他们的尸检研究表明,斑块在认知症状出现前多年就已形成。
艾森说,该领域并没有忽视寻找治疗有症状阿尔茨海默病的方法的重要性。但临床研究人员现在正将更多注意力转向治疗症状前阿尔茨海默病的药物试验。然而,为这些试验寻找参与者并不容易。人们需要没有症状,但极有可能在可测量的时限内开始出现症状。识别这些个体有两种方法:找到像雷斯维格这样具有罕见遗传易感性的人,或者在普通人群中找到因大脑中存在淀粉样蛋白 β 而患阿尔茨海默病风险较高的人。
为了识别罕见的遗传病例,美国国家老龄研究所 (NIA) 于 2008 年在马里兰州贝塞斯达资助启动了显性遗传阿尔茨海默病网络 (DIAN)。它现在包括来自 20 个国家的 600 多人,代表大约 300 个家庭,这些家庭携带与早发性阿尔茨海默病相关的三个基因之一的突变。每个家庭成员有 50% 的机会遗传突变。
该网络迅速聚集了更多资金和研究合作伙伴,并开始招募家庭(包括雷斯维格的家庭)参与观察计划。研究人员定期进行脑部正电子发射断层扫描 (PET) 以检查淀粉样蛋白 β 和其他阿尔茨海默病生物标志物,并将携带基因的家庭成员与不携带基因的家庭成员进行比较。他们还记录了每个家庭中症状开始出现的时间。该网络 2018 年的报告证实,淀粉样蛋白异常的最初迹象在症状开始前长达 25 年就会出现。
DIAN 联盟于 2012 年开始了一项为期七年的淀粉样蛋白结合抗体试验。该试验旨在延缓那些没有认知症状但已开始在其大脑中出现阿尔茨海默病主要标志物——淀粉样蛋白斑块——的人的疾病进展。该试验招募了 194 名处于不同疾病阶段的参与者,并将他们分成几组,分别接受两种抗体之一 gantenerumab 或 solanezumab,或安慰剂。
但 2020 年公布的试验结果令人失望。该试验未能证明这些药物可以减缓认知能力下降——尽管接受治疗的症状前参与者的认知能力下降很少,但安慰剂组的认知能力下降也很少。“这意味着我们根本无法说这些药物最终是否会对无症状人群有所帮助,”圣路易斯华盛顿大学医学院的兰德尔·贝特曼说,他领导着进行这项研究的 DIAN 试验部门。
尽管如此,其中一种抗体 gantenerumab 对该疾病的生物标志物产生了显着影响。它不仅减少了淀粉样蛋白斑块,还降低了 tau 蛋白的水平和另一种神经退行性变标志物(一种在血液中出现的神经元蛋白)的水平。
这些结果鼓励贝特曼和 DIAN 联盟继续研究 gantenerumab 另外三年,放弃 solanezumab 和安慰剂组,但允许这些组中的参与者转换为 gantenerumab,并让他们知道他们正在服用哪种药物。
这给雷斯维格带来了两难境地。当他最初接受基因突变检测时,他选择不被告知结果。但该研究的扩展仅适用于突变携带者,因此参与请求将自动揭示他的基因状况。“我决定是时候让我知道了,但我仔细计划了一切,”他说。他与妻子一起退居到科罗拉多州的一个度假租赁屋,接听来自他的遗传咨询师的电话。“我不想在自己家里知道结果——这至少是我想要控制的事情。”当雷斯维格得知自己携带突变时哭了,并决定他唯一的机会是继续参加试验。
去年,该联盟决定尝试治疗大脑中没有认知症状也没有斑块的人。“这将真正成为阿尔茨海默病预防的终极试验,”贝特曼说。在接下来的几个月中,该团队计划开始招募 160 名突变携带者,其中一些人年仅 18 岁,预计在未来 11-25 年内不会出现症状。安慰剂对照试验将持续四年,定期监测人们的淀粉样蛋白状况。然后,它将进入为期数年的“开放标签研究”:安慰剂组将被取消,所有参与者都将接受试验药物。届时,它还将测量疾病进展的其他生物标志物。
华盛顿大学圣路易斯分校的试验首席研究员埃里克·麦克戴德说,对于参与者来说,要运行数十年才能出现症状的试验是不切实际的。相反,该团队将监测生物标志物的变化,例如淀粉样蛋白 β 和 tau 蛋白,这些生物标志物现在已知可以预测该疾病漫长沉默期内的症状发作。“我们可以改变的这些其他生物标志物越多,我们抵消或至少显着延迟发作的可能性就越高。”他说,研究人员将在试验的第二阶段之后继续监测尽可能多的参与者。
在 DIAN 联盟之外,其他针对早发性阿尔茨海默病的试验正在进行中,在已经有一些淀粉样蛋白积聚的人身上测试药物。Genentech-Roche 正在研究哥伦比亚一个大家庭的成员,其中一半人携带一个基因的病理性突变,该基因编码一种淀粉样蛋白切割分泌酶的一部分。其药物 crenezumab 的试验将于今年完成。在唐氏综合征患者中测试阿尔茨海默病药物的研究也在准备中。
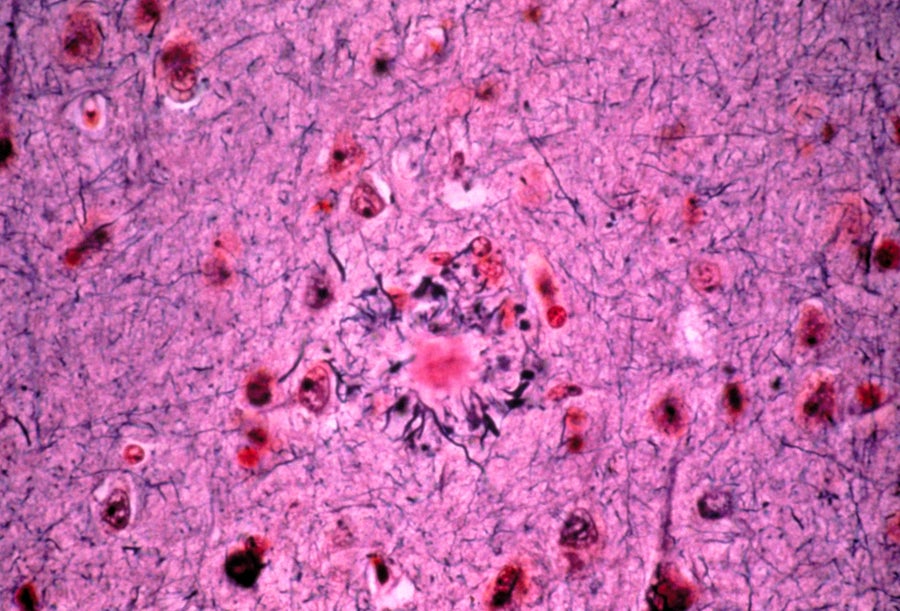
淀粉样蛋白斑块(中心)显示在患有阿尔茨海默病的人的脑组织中。图片来源:Martin M. Rotker/SPL
阻止症状
预防性试验的第二种方法是识别普通人群中患晚发性阿尔茨海默病的高危人群。国际阿尔茨海默病神经影像学倡议是一项总部位于加利福尼亚大学旧金山分校的公私合作项目,通过正常衰老和疾病的各个阶段追踪数百人的阿尔茨海默病生物标志物。其数据显示,大约三分之一 65 岁以上认知正常的人的大脑中都有淀粉样蛋白斑块,其中超过 85% 的人将在 10 年内发展出阿尔茨海默病症状。
在此基础上,正在进行三项大型安慰剂对照临床试验,每项试验招募 1000 多名认知能力良好但通过 PET 扫描发现大脑斑块的人。每项试验都在测试一种不同的抗体。所有三项试验都将持续四年,到那时,在斑块开始积累后,通常可以测量到认知能力下降。
艾森的研究所正在协调 A4 试验——无症状阿尔茨海默病中的抗淀粉样蛋白治疗——该试验正在测试礼来公司的药物 solanezumab。预计明年公布结果。艾森还共同领导了 AHEAD 3-45 试验,该试验于 2020 年开始,正在测试 lecanemab。同年,礼来公司启动了一项名为-Alz 2 的 donanemab 试验。今年,罗氏公司将启动其自身的 gantenerumab III 期试验,该试验将持续六年。
艾森说,此类试验的成本“通常高达数亿美元”。仅招募 A4 试验中的 1,169 名参与者就需要大约 4,500 次 PET 扫描,每次扫描的平均成本为 7,000 美元。“但是,这种疾病给社会带来的痛苦、死亡率和经济影响方面的成本证明了对有效治疗进行巨额投资是合理的,”他说。
近年来,在开发更简单的、基于血液的阿尔茨海默病生物标志物方面取得了重大进展。其中两项预防试验正在使用此类生物标志物来帮助选择进行 PET 筛查的人员,从而降低 PET 扫描的成本和参与者的不便。一种生物标志物测量两种略有不同的淀粉样蛋白 β 形式的比率,另一种生物标志物测量一种与 tau 相关的分子。
到目前为止,预防性试验都使用针对淀粉样蛋白 β 的抗体。这些药物有两个缺点。它们可能会产生副作用:少量脑出血或肿胀,这些大多是无害的,但也可能是严重的。而且它们很昂贵。Biogen 最初将其 aducanumab 一年治疗的定价定为 56,000 美元,尽管它在 2021 年 12 月将其减半。
但该领域正在考虑重新审视更简单的小分子药物,这种药物的生产成本远低于基于抗体的疗法。艾森说,一些公司正开始考虑重新审视分泌酶,也许会调整早期试验中失败的酶阻断分子的结构,或者找到更好的给药方法。
复杂的原因
该领域的研究人员意识到,解决痴呆症问题还需要付出超出淀粉样蛋白 β 的努力。“阿尔茨海默病更复杂,”瑞士苏黎世大学 aducanumab 的原始开发者之一、神经生物学家罗杰·尼奇说。“淀粉样蛋白是一种非常缓慢燃烧的神经毒素,它会引发疾病,但脑细胞——包括连接血管和免疫系统细胞的脑细胞——会反击。”他说,将会有更多方法来靶向已确立的疾病。此外,所有痴呆症中只有大约三分之二属于阿尔茨海默病类型,尸检研究表明,其中一半具有混合病理——大脑除了淀粉样蛋白和 tau 蛋白外,还含有其他毒性蛋白质,或血管损伤的迹象。
NIA 主任理查德·霍德斯说,预防性试验非常重要且前景广阔,“但我们不会放弃已经患病的人”。他说,因为即使在同一个人身上,也可能有多种因素导致痴呆症——因此需要一系列治疗方法。美国国家老龄研究所正在资助 72 项痴呆症临床试验,试验针对各种靶点的药物。例如,一些旨在降低血压以减少大脑中小血管破裂的风险;另一些则靶向 tau 蛋白。只有 20 项靶向淀粉样蛋白。美国国家老龄研究所还支持至少 120 项试验,以研究非药物干预措施的影响,例如认知训练、锻炼和饮食。
研究人员估计,2021 年,全球临床试验中正在研究至少 126 种不同的制剂——包括 NIA 研究中的制剂。
作为一名志愿者,雷斯维格不得不接受他的特殊试验带来的特殊负担——不仅是时间投入,还有不断提醒他,如果试验药物不起作用,等待他的命运。他说,DIAN 联盟每年将来自世界各地的参与者聚集在一起分享他们的经验,这对他们有所帮助。“我们创建了一个美好的社区,我们知道我们为科学做出了巨大贡献。”
本文经许可转载,并于 2022 年 3 月 9 日首次发表。
