当医生让莎拉·格里格描述她的疼痛时,她经常说那是难以形容的。刺痛、灼痛、酸痛——这些词语常常无法描绘出已经持续如此之久的感觉,以至于它们现在已成为她身体的一部分,就像她的骨骼和皮肤一样。“我的疼痛就像一个额外的肢体,每天都伴随着我。”
格里格是一位前瑜伽教练和私人教练,居住在威斯康星州,今年 40 多岁。17 岁时,她发现自己患有脊椎管狭窄症,这是一种脊髓狭窄,会压迫那里的神经。她经历了背部、臀部以及腿部放射性剧烈疼痛的爆发。多年来,尽管她尝试通过物理疗法、消炎注射和多次手术来阻止疼痛,但疼痛还是蔓延开来。布洛芬(Advil)等非处方药几乎无法缓解疼痛。而且她对最强效的止痛药——处方阿片类药物——过敏,这些药物会引起剧烈的呕吐。
如今,她的痛苦通常徘徊在标准数字疼痛等级的 7 级(0 级为无痛,10 级为最严重的疼痛)。偶尔,她的疼痛会爆发到 9 级或 10 级。在她的医生说服她服用抗抑郁药之前,格里格一度与自杀念头作斗争。“对于许多患有慢性疼痛的人来说,疼痛总是如影随形,”她说。“并不是我们想死。我们只是想让疼痛消失。”
支持科学新闻报道
如果您喜欢这篇文章,请考虑通过以下方式支持我们屡获殊荣的新闻报道: 订阅。通过购买订阅,您将帮助确保关于塑造我们当今世界的发现和思想的具有影响力的故事能够继续存在。
格里格说她愿意尝试另一种止痛药,但前提是她知道它是安全的。她密切关注最新的研究,因此她很想在 2024 年听到 Vertex Pharmaceuticals 正在测试一种与阿片类药物和其他止痛药作用机制不同的新药。
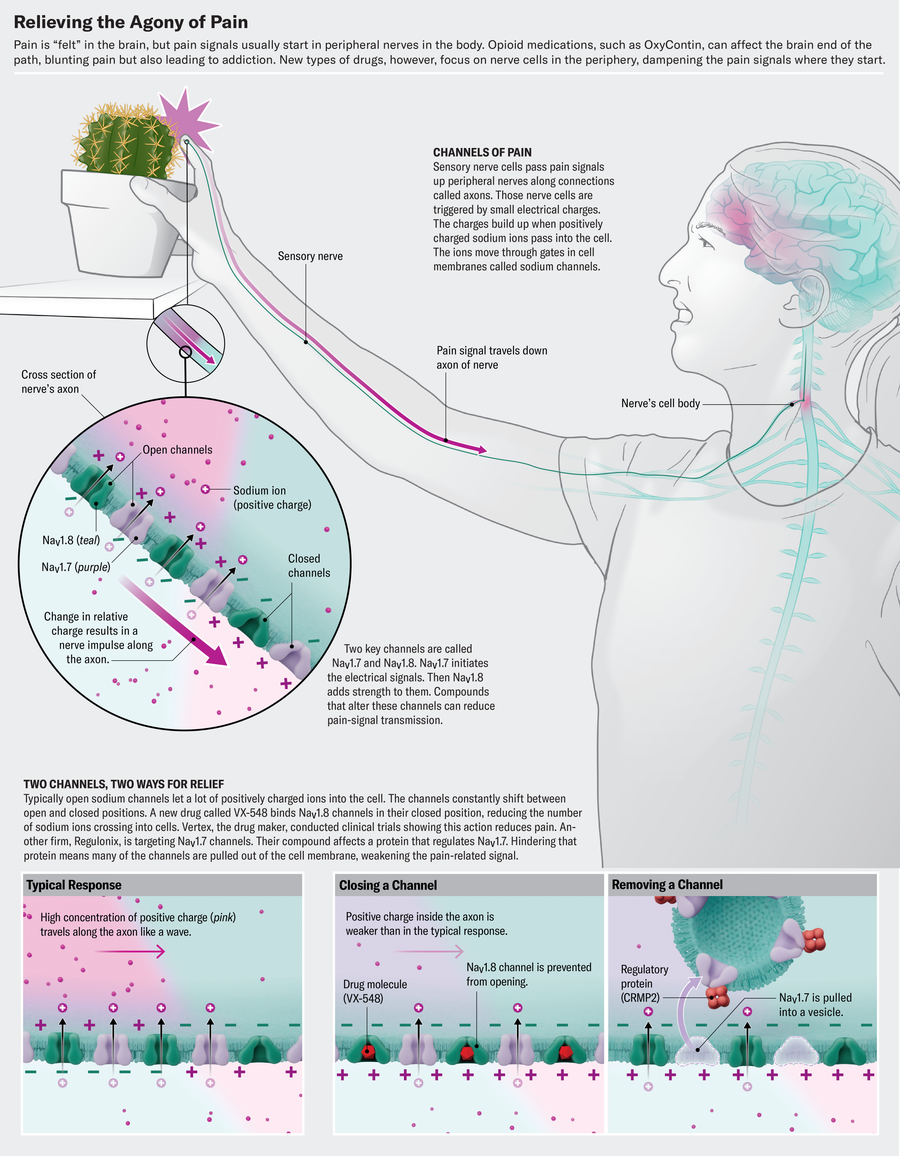
这种名为 VX-548 的药物是一种药丸,它可以阻断疼痛信号,使其无法到达大脑。它会阻塞周围神经细胞中的钠通道,而受阻的通道使这些细胞难以传递疼痛感。由于该药物仅作用于周围神经,因此它不会像阿片类药物那样具有成瘾性——羟考酮(OxyContin)和类似药物会对大脑和脊髓产生影响,因此会触发大脑的奖励中心和成瘾循环。
一位巴基斯坦年轻的走火者有一种影响疼痛信号神经元的基因突变,使这个男孩可以在燃烧的煤炭上行走而感觉不到疼痛。
2024 年 1 月,Vertex 宣布了 VX-548(现称为 suzetrigine)临床试验的喜人结果,表明该药将急性疼痛水平降低了大约一半(以 0 到 10 分制计算)。该公司同年向美国食品和药物管理局 (FDA) 申请批准该药物。
其他针对钠通道的止痛药目前也在开发中,其中一些公司受到 Vertex 成功的激励。由生物医学工程师安娜·莫雷诺领导的 Navega Therapeutics 甚至正在使用 CRISPR 等分子编辑工具来抑制与慢性疼痛相关的基因。“我们绝对希望能够取代阿片类药物,这就是我们的目标,”她说。
在美国,每五名成年人中就有一人(截至 2021 年为 5160 万人)患有慢性疼痛。新发病例比其他常见疾病(如糖尿病、抑郁症和高血压)更频繁。然而,疼痛治疗的进展并没有跟上需求的步伐。市面上有阿司匹林、对乙酰氨基酚(泰诺)和非甾体抗炎药 (NSAID)(如 Advil)等非处方药。还有阿片类药物。现有药物在缓解人类痛苦方面的明显不足加剧了持续不断的阿片类药物流行,自其开始以来,已导致超过 73 万人死于过量服用。
VX-548 确实存在局限性。它让一些患者感到明显不适,而且到目前为止,它主要在急性疼痛患者中进行了测试,而不是在更大的慢性疼痛问题中。格里格说,她希望在服用该药之前获得更多关于该药不会引起不良副作用的保证。
但耶鲁大学研究疼痛信号的神经学家斯蒂芬·韦克斯曼(Stephen Waxman)表示,这种化合物表明,新的止痛机制是可能的——他没有参与 Vertex 的临床试验。他指出,未来使用这种机制的药物可能会更有效。韦克斯曼过去常常告诉患者,一种新的疼痛管理方法即将问世,但可能需要很多年才能实现。“现在我可以放宽限制,说我认为事情很快就会发生,”他说。
如今存在的止痛药在很大程度上是数千年来一直存在的天然产物的衍生物。阿司匹林最初来自柳树皮。吗啡和可待因源自罂粟植物。早在 4000 年前,古代苏美尔人就将演变成两大类止痛药——NSAID 和阿片类药物——的处方刻在泥板上。
过去二十年进行的关于疼痛分子机制的现代研究使另一种方法成为可能。科学家们知道,我们的身体内有大量的疼痛信号神经细胞,这些细胞支配着我们的皮肤、肌肉和内脏组织。这些细胞就像一个警报系统,可以检测到威胁性刺激,例如极端温度、尖锐物体或有害化学物质。为了响应这些信号,它们会产生脉冲,将疼痛信号沿着神经纤维传递到位于脊髓旁边的背根神经节细胞簇。从那里,信号继续向上到达大脑,在那里疼痛变成现实。“这就是疼痛轴,”佛罗里达大学药理学家和疼痛研究员拉杰什·卡纳(Rajesh Khanna)说。
钠通道是该通路的核心,它是分散在神经细胞膜上的细胞门。每当膜电位发生变化时,这些门就会打开,允许钠离子涌入,从而产生负责神经冲动的电流。通常,这些疼痛信号具有保护作用——提醒人们将手从滚烫的炉子上移开,或注意到需要解决的炎症或损伤。但在慢性疼痛中,这些保护机制可能会出错。
电压门控钠通道(或 NaV,Na 代表钠,V 代表电压)似乎是治疗疼痛的理想靶点;毕竟,如果你能阻止它,你就能阻止疼痛信号的传递。然而,由于这些通道控制着为心脏和大脑提供动力的电脉冲,因此随意阻断它们会损害重要功能。这就是为什么普鲁卡因和利多卡因(它们都是钠通道阻滞剂)被用作局部麻醉剂,但如果全身给药,可能会引起严重的副作用。因此,试图阻断这些疼痛通路的科学家们寻找在周围感觉神经中更频繁地发挥作用的通道,最终确定了三个:NaV1.7、NaV1.8 和 NaV1.9。
NaV1.7 和 NaV1.8 是疼痛信号传导的关键参与者。“它们像多米诺骨牌一样协同工作,”韦克斯曼说。“NaV1.7 启动电信号,NaV1.8 接管,产生 80% 的动作电位基础电流。”(NaV1.9 在设定疼痛信号神经元的阈电位方面发挥着更小的作用。)
大约从 20 年前开始,一系列报告将这些通道与人类的疼痛障碍联系起来。在中国一个患有罕见疾病——红斑性肢痛症或“火人综合征”——的家庭中,发现了一种编码 NaV1.7 的 SCN9A 基因突变。患有这种疾病的人,轻微的温暖就会引发灼痛发作,感觉就像喷枪一样。韦克斯曼发现,红斑性肢痛症患者的突变使 NaV1.7 通道过度活跃,导致疼痛信号神经元“在应该低语时尖叫”。在其他地方,研究人员在一位巴基斯坦年轻的走火者身上发现了一种作用相反的突变。这种突变消除了疼痛信号离子通过 NaV1.7 通道的流动。因此,这个男孩可以在燃烧的煤炭上行走而感觉不到疼痛。
对他病情的遗传基础的发现(被称为先天性痛觉不敏感症)在制药行业掀起了一场竞赛,以寻找可以阻断 NaV1.7 的分子。目标是为其余人群提供类似的无痛生活。“这就是圣杯。你有一个蛋白质,你突变它,你就没有疼痛——它一定是靶点,”卡纳说。“许多制药公司为此投入了大量资金,但这些化合物都没有成功。”
许多靶向 NaV1.7 的化合物在实验室中看起来很有希望,但在临床试验中却失败了。制药公司阿斯利康和基因泰克都开发了在 1 期试验后停滞的候选药物。辉瑞的 PF-05089771 在一系列诱发健康志愿者疼痛的测试中未能发挥作用。Biogen 在几种神经性疼痛类型的 2 期试验中获得平淡的结果后,放弃了其 NaV1.7 抑制剂 vixotrigine 的开发。经过十多年的虚假启动,投资减少,候选药物从开发管道中消失。
“对于许多患有慢性疼痛的人来说,疼痛总是如影随形。并不是我们想死。我们只是想让疼痛消失。”——莎拉·格里格,疼痛患者
2017 年,白宫宣布阿片类药物危机为公共卫生紧急事件,这场危机每天导致 91 人丧生。同年,时任美国国立卫生研究院院长的弗朗西斯·柯林斯召集了行业领导者以及基础科学家和临床医生,讨论应对危机的策略。当时领导生物制药巨头安进公司研发部门的肖恩·哈珀回忆说,会议有来自全球约 20 家顶级制药公司的代表参加,柯林斯询问他们有哪些在研药物。“这很令人难过,”哈珀回忆道。“除了防篡改、防压碎的阿片类药物药丸外,很少有公司在研究其他任何药物。”
整个行业的新型止痛药研究停滞不前。安进公司已经确定了许多潜在的 NaV1.7 抑制剂,但最终不仅关闭了其疼痛研究,还关闭了其大部分神经科学项目。总的来说,“我认为发生的事情是人们觉得这太难了,”哈珀说。
困难的一个重要原因与靶点本身的性质有关。NaV 通道家族包含九个密切相关的成员,它们的基因序列共享超过 50%。由于这种相似性,2000 年代开发的钠通道抑制剂通常无法在不影响其他亚型的情况下靶向一种亚型。“坦率地说,选择性很差,”旧金山生物技术公司 SiteOne Therapeutics 的化学家兼首席执行官约翰·马尔卡希(John Mulcahy)说。“克服这个问题需要很长时间。”
在 Vertex,研究人员认为,之前测试过的化合物只是选择性不够好,或者与通道结合的时间不够长,要找到有效的分子,他们只需要继续搜索。为了加快搜索速度,他们一直在研究一种技术,该技术可以测量大量分子在不同浓度下对几种钠通道的开放和关闭的影响。传统上,研究人员使用一种称为膜片钳电生理学的费力方法来研究钠通道。该技术包括分离细胞膜的一部分,施加电压以触发其通道打开,添加一种潜在的药物,然后记录电活动的振荡波。
在 2000 年代初期,Vertex 科学家赫苏斯·冈萨雷斯(Jesús González)和迈克尔·马赫(Michael Maher)设计了一个名为 E-VIPR(电刺激电压离子探针读取器)的系统,以非常快速地测试针对一个通道的多种化合物。该系统使用高密度细胞阵列,每个细胞阵列表达一种钠通道类型。微小的电极产生电场,可以每秒刺激通道多达 100 次。当这些通道打开时,电压敏感染料会从橙色变为蓝色,颜色变化由精密的 оптическое 检测工具捕获。
Falconieri Visuals
Vertex 高级副总裁兼疼痛项目负责人保罗·内古列斯库(Paul Negulescu)说:“这是一个非常快速的过程,比人眼可以检测到的速度还要快,但信息量非常丰富。”工程团队大约在 20 年前开发了第一代技术,现在是第三代技术。“这就是主力。我们已经在每天运行的系统上测试了数万种化合物,”他补充道。
通过这种方法,Vertex 可以广泛测试一种潜在药物如何与特定通道相互作用。钠通道在打开和关闭时会经历巨大的形状变化,蛋白质碎片以惊人的速度上下移动。“这有点像一匹烈马,”内古列斯库说。“药物必须跳上烈马,并在它经历各种步伐时保持在上面,并最终让这匹烈马平静下来,停止移动。”一种候选药物可能会在通道上停留一段时间,但一旦它的旋转被证明太过分,就会被踢下来。或者它可能会跳到另一个通道上,产生不需要的脱靶效应。
内古列斯库说,Vertex 的方法试图模拟钠通道的生理状态,使其经历多次打开和关闭循环,以确保任何有希望的新药都能保持原位。“大多数方法都不是这样做的,”他说。“正因为如此,我相信当我们接触到人时,我们最终得到的药理学无法转化。”该公司使用其专有方法生成了关于各种不同钠通道的数据。当行业继续关注 NaV1.7 时,Vertex 开始在 NaV1.8 上看到成功,并推进了一个关于被忽视通道的项目。“我认为当其他人 zagged 时,我们 zigged,”内古列斯库说。
Vertex 于 2015 年启动了其首个 NaV1.8 抑制剂的临床试验。效果不够好,紧随其后的两个抑制剂效果也不好。但最终,其中一种抑制剂被一小部分患者良好耐受,并缓解了他们的一些疼痛。这就是 VX-548,它促使该公司在 2022 年推进了更大规模的研究。
两年后,即 2024 年 1 月,Vertex 宣布了两项大型关键临床试验的积极结果。研究人员招募了约 1100 人,他们每个人都接受了拇外翻切除术或腹部除皱术,这些手术通常用于模拟急性疼痛。研究参与者接受了安慰剂、VX-548 或氢可酮(一种阿片类药物)和对乙酰氨基酚(即维柯丁)的药物组合。
当使用 0 到 10 分制疼痛等级测量疼痛缓解程度时,新药的表现与维柯丁一样好,而且没有成瘾风险。两种治疗方法都将疼痛降低了约 3 分,从约 7 分降至 4 分。在腹部手术后康复的人群中,VX-548 起效比服用维柯丁的人更快。
当使用不同的疼痛等级时,该药物对拇外翻切除术患者的缓解效果不如维柯丁。尽管如此,服用 VX-548 的患者报告的副作用(如恶心、便秘、头痛和头晕)比服用安慰剂的患者少,表明该治疗通常是安全的。(安慰剂组中未治疗的疼痛可能会增加副作用,因为它会增加压力水平,扰乱消化或引发头痛。)
研究表明,即使疼痛降低 3 分,也可能对生活质量产生有意义的影响。威斯康星州患者格里格回忆说,有一次她的疼痛等级为 4 级,她能够工作。在一次拙劣的手术使她的疼痛飙升后,她被迫领取残疾救济金。
如果获得批准,VX-548 可以通过提供介于对乙酰氨基酚等药物(安全但效力有限)和更强的阿片类药物(带有严重风险)之间的缓解,来帮助像格里格这样的人。它可以为对其他药物过敏或根本无法耐受其他药物的患者提供缓解。此外,它可以为想要避免药物依赖风险的个人提供选择。
Vertex 已向 FDA 申请批准该药物用于中度至重度急性疼痛病例。许多专家一致认为,尽管首先针对急性疼痛在实验上是有道理的,但更大的需求是为日常生活受到慢性疼痛干扰的人们提供缓解。Vertex 科学家认为,该药物对那种痛苦有效,因为慢性疼痛和急性疼痛的基础机制相似。它报告了 VX-548 在糖尿病周围神经病变(一种由高血糖引起的神经损伤引起的常见慢性疼痛类型)中的一项较小的有效性和安全性试验的积极结果,并计划推进 3 期试验。
此外,该公司还启动了一项单独的研究,测试该药物在一种称为腰骶神经根病变的慢性下背痛形式中的作用。Vertex 研究人员继续使用其药物发现平台来开发更有效和更具选择性的化合物。“我们所做的一切都是为了持续创新,”内古列斯库说。该公司已经有一种下一代 NaV1.8 抑制剂 VX-993,正在向 2 期临床试验迈进。
疼痛领域的其他人一直在密切关注 Vertex,并对其结果感到兴奋。“我认为 Vertex 在这里做出的巨大贡献,即利用他们的项目生成他们拥有的临床数据,是为了让人们明白,嘿,这并不是一件毫无希望的事情,”哈珀说。他与其他投资者最近成立了一家名为 Latigo Biotherapeutics 的公司,以开发钠通道抑制剂。
韦克斯曼说,Vertex 的发现是适度的,但很重要——非常重要,以至于他称 VX-548 为“游戏规则改变者”,不是因为它本身会改变临床实践,而是因为它将改变研究管道。“这将像他汀类药物的开发一样,”他说。“回顾过去,第一批他汀类药物并不是很好。但它们奠定了基础,并且确实是动力,我们现在拥有的药物正在改变生活。”
只有少数几家公司公开开发针对 NaV1.8 或 NaV1.7(仍然是一个可行的靶点)的疼痛治疗药物。可能有更多公司在“隐身”状态下工作(默克的专利活动表明它正在涉足该领域),而另一些公司很可能会加入这项工作,并受到 Vertex 进展的鼓舞。一些公司已经在设计小分子来阻断钠通道或附近的蛋白质;一些公司正在修改天然毒素以禁用疼痛信号的传输;还有一些公司正在使用基因疗法来降低源头的信号。
哈珀的初创公司 Latigo 是该领域最新出现的公司。2024 年 2 月,这家总部位于加利福尼亚州的生物技术公司以 1.35 亿美元的资金和一种 NaV1.8 抑制剂 LTG-001 启动了 1 期临床试验。早期,该公司同时追求 NaV1.7 和 NaV1.8。但哈珀说,当它看到 Vertex 的一种候选药物在急性和慢性疼痛模型中都取得了积极成果时,这“有助于将 NaV1.8 推到队列的前面”。现在 Latigo 还有一些其他小分子正准备进行测试。哈珀指出,通常当一家公司像 Vertex 一样将一种全新的药物类别引入临床时,就会有许多其他人“紧随其后”。
哈珀说,以前,由于历史上对止痛药的投资不足,导致“竞争相当缓和”。根据生物技术行业贸易组织 BIO 的一项分析,考虑到这些疾病给社会带来的负担,对疼痛和成瘾药物开发的投资非常低。2021 年,疼痛和成瘾公司筹集了 2.28 亿美元的风险投资。这仅占美国治疗性风险投资总额的 1.3%。相比之下,肿瘤公司获得了 97 亿美元,占风险投资总额的 38.3%。更重要的是,大多数行业疼痛项目都集中在阿片类药物的不同配方上,而不是冒险涉足新的机制。
美国国家神经疾病和中风研究所临床前疼痛研究办公室主任迈克尔·奥辛斯基(Michael Oshinsky)表示,制药公司持续关注阿片类药物而忽视其他研究途径的一个主要原因是,阿片类药物一直是更安全的选择。“阿片类药物的临床试验有 30% 的机会进入市场。对于治疗药物开发来说,这真的非常高。而对于不影响阿片受体的药物来说,这个机会约为 0.7%,”他说。
奥辛斯基与人共同主持了 NIH 的“帮助结束长期成瘾 (HEAL)”倡议,该倡议旨在加速对新型非成瘾性止痛药的研究。“我们所做的是努力降低靶点的风险,”他说。该计划一直在帮助像 Regulonix、SiteOne 和 Navega 这样的新兴钠通道抑制剂开发商,方法是验证他们的靶点、优化他们的化合物或在临床前模型中测试他们的方法。
当使用 0 到 10 分制疼痛等级测量疼痛缓解程度时,新药的表现与维柯丁一样好,而且没有成瘾风险。
亚利桑那大学的分拆公司 Regulonix 坚持将 NaV1.7 作为靶点,但其方法与之前的公司不同。该公司不是阻断钠通道,而是试图从细胞膜上去除 NaV1.7。如果没有通道,可以穿过细胞的钠离子就会减少。佛罗里达大学的卡纳是 Regulonix 的联合创始人兼首席科学官,他说,其化合物的早期版本成功地影响了急性疼痛和慢性疼痛的大鼠、小鼠和猪模型中的 NaV1.7 信号传导。但是,他承认,“我们离人体试验还差得很远。”
另一种方法是采用天然存在的钠通道阻滞剂——例如使河豚如此致命的河豚毒素——并对其进行改造,以阻断主要存在于疼痛感知神经元中的通道。斯坦福大学科学家创立的 SiteOne 正在遵循这一计划。2022 年,它开始与 Vertex 合作开发其靶向 NaV1.7 的治疗候选药物。该公司还获得了 NIH 的额外资金,用于研究一种名为 STC-004 的 NaV1.8 抑制剂。“根据我们的经验,NaV1.7 抑制剂几乎可以像疼痛的开关一样,”马尔卡希说。但是 NaV1.8 药物“有点不同——它更像是一个调光开关。”
最后,一些研究人员并没有操纵现有的疼痛通道,而是试图通过降低编码它们的基因的活性来阻止形成如此多的疼痛通道。莫雷诺及其公司 Navega 正在追求这种类型的基因疗法。他们正在使用莫雷诺在加州大学圣地亚哥分校攻读博士学位期间开发的一项技术。在那里,她使用了 CRISPR 及其较旧的基因编辑对应物锌指蛋白来靶向有助于构建 NaV1.7 的基因;结果是抑制甚至预防了啮齿动物的疼痛。自从成立 Navega 以来,她和她的团队已经证明,该方法适用于各种疼痛——包括神经性疼痛、化疗引起的疼痛、炎症性疼痛、内脏疼痛和关节炎性疼痛——他们正在迅速推进首次人体试验。
莫雷诺说:“由于我们获得了持久的效果,我们将专注于难治性疼痛。” Navega 计划在更大、更复杂的慢性疼痛临床试验之前,在那些患有已知突变导致疼痛的罕见“火人综合征”患者亚群中测试基因疗法。“我们一直收到来自世界各地受苦患者的电子邮件,”她说。“这非常有动力。”
对于格里格来说,在她的药箱中添加一种新型有效止痛药的前景给了她希望。但她以前也尝试过新事物,但最终因严重的副作用而受挫。格里格说,她会等到她的医生向她保证 VX-548 是安全的时候再尝试。她说,显示副作用很少的试验很重要,但她更希望该药物在临床使用一段时间后再亲自服用。
目前,她依靠其他方法来应对疼痛。她为美国疼痛基金会运营着六个支持小组,包括一个 LGBTQ 社区小组和一个威斯康星州居民小组。在多年尝试其他一切方法之后,她从每天的反思和祈祷、正念和冥想的练习中体验到了最大的疗愈。“这是一种每天不断倾听我的身体,真正努力学习自爱和自怜——这就是我的药物,”她说。她的自我疗愈实践让她坚持下去。但她不介意从医学界获得更多帮助。
如果您需要帮助
如果您或您认识的人正在与自杀念头作斗争,请寻求帮助。拨打 988 自杀与危机生命线 988,或使用在线生命线聊天 988lifeline.org/chat,或发送短信 TALK 至 741741 联系危机短信专线。

