索菲告诉我,记忆力衰退就是这样开始的:你上班时,忘记了本应与客户共进早餐会议。你记不起邻居的名字。很快,你走进一个房间,却不知道自己为什么在那里。索菲是一位 50 岁出头的律师,她要求使用化名。她一直饱受潮热和盗汗的困扰,这两种症状都与更年期有关,但健忘似乎是另一回事。她的头脑到底发生了什么事?
丽莎·莫斯科尼是女性大脑倡议主任,也是纽约市威尔康奈尔医学院阿尔茨海默病预防中心的副主任,她或许知道答案。她分析了数千张进入更年期患者的 позитрон-эмиссионная томография (PET) 扫描图,并观察到她们的大脑代谢随时间变化的情况。“在绝经前期,你的大脑能量很高,”莫斯科尼一边说,一边向我展示一位年轻女性大脑的 PET 扫描图。扫描图上亮起了许多鲜红和橙色的斑点,代表着高葡萄糖代谢——神经元活动的指标。在围绝经期,女性通常在 40 岁中期到后期进入这个阶段,大脑葡萄糖代谢减慢 10% 到 15% 或更多,扫描图也会发生变化:红色和橙色斑点让位于更多的黄色和绿色,代表着葡萄糖吸收减少和代谢降低。“然后,在绝经后期,大脑葡萄糖代谢减慢 20% 到 30%,有时甚至更多,”莫斯科尼一边说,一边向我展示了最后的扫描图。现在,很明显,绿色已经扩大了地盘。
雌激素是年轻女性大脑代谢的主要调节器,它协调着从葡萄糖转运和摄取到分解供能的一切过程。莫斯科尼的扫描图是彩虹色的证据,表明更年期期间激素水平下降(通常发生在女性 45 岁到 55 岁之间)会导致她所描述的“生物能量大脑危机”。在这个长达七年以上的过渡期中的某个阶段,高达 60% 的女性会经历所谓的更年期相关认知障碍:阵发性意识模糊、注意力不集中和健忘。这些记忆问题是正常的。突触的生成需要能量;随着雌激素水平和大脑葡萄糖代谢的下降,神经元之间新连接的形成也会减少。
支持科学新闻报道
如果您喜欢这篇文章,请考虑支持我们屡获殊荣的新闻报道,方式是 订阅。通过购买订阅,您将有助于确保有关塑造我们当今世界的发现和想法的具有影响力的故事能够拥有未来。
幸运的是,这种障碍是暂时的:女性会恢复,她们的才智完好无损,因为大脑会进行补偿并利用其他能量来源。2009 年的一项研究发现,新进入绝经后期的女性在认知测试中的得分与过渡期之前一样好。然而,几十年后,大约五分之一的女性将被诊断出患有阿尔茨海默病。莫斯科尼和其他人认为,对于仅在美国就有 360 万患有这种疾病的女性来说,更年期可能是认知能力下降的临界点。
尽管专注于女性阿尔茨海默病的研究已成为首要任务,但在女性特有的疾病风险因素、症状、预防和治疗反应方面,仍有太多问题没有解答。为什么在美国,女性在 65 岁时患这种疾病的终生几率为五分之一,而男性在同一年龄段的几率仅为九分之一?美国女性的平均寿命比男性长五年,但“长寿并不能完全解释患病频率和终生风险较高的原因”,代表妇女健康研究协会的专家组在 2018 年的一项分析中指出。为什么携带基因 APOE (APOE4) e4 变异体的女性(这种变异体会增加阿尔茨海默病的风险)比男性携带者更容易在更年轻的时候患上这种疾病?女性的生物学和生活经历中到底是什么因素使她们更容易受到伤害?
更年期假说——即这一时期雌激素水平的下降使大脑容易受到未来损害——可能提供答案。如果莫斯科尼和其他研究人员是对的,那么索菲和全世界数百万正在经历这一过渡期的女性可能会从生活方式干预中受益,并且可能但有争议地,可以从激素疗法 (HT) 中受益,以预防这种疾病。
雌激素减少时的思考
“这是一种饥饿模式,”亚利桑那大学大脑科学创新中心主任罗伯塔·迪亚兹·布林顿在描述更年期女性的 PET 扫描图中雌激素下降和绿色斑块占据主导地位时说道。她解释说,雌激素在大脑生物能量学中发挥着多种且广泛的作用。作为一种在整个大脑中都有受体的信号分子,它调节线粒体,线粒体为细胞产生能量,并为神经元连接的形成提供燃料。雌激素还激活使突触发挥功能的酶,并促进葡萄糖从血管进入大脑,以及从大脑进入神经元和神经胶质细胞(支持和保护神经元的细胞)。
布林顿对衰老雌性小鼠的研究表明,随着雌激素水平下降和葡萄糖代谢减慢,大脑会通过使用酮体(由脂肪酸产生的物质,在这种情况下来自白质,包括保护神经元的髓鞘)作为补充燃料来源来适应。这种转换——本质上是一种自我蚕食的行为——似乎也在一定程度上发生在女性身上,而那些大脑更严重地依赖酮体的女性可能会遭受更严重的白质退化和更高的痴呆症风险。
有时,大脑能量不足与 β-淀粉样蛋白的硬沉积物或斑块的形成同时发生。它们可能会出现在一些功能正常的大脑中,但每个阿尔茨海默病患者都有这些斑块。人们认为它们会干扰突触信号传递。在患有这种疾病的人的大脑中,β-淀粉样蛋白通常与 tau 蛋白同时出现,tau 蛋白是一种缠绕在细胞核内的蛋白质,显然是通过阻止营养物质运输来杀死细胞。此外,低雌激素会增加血脑屏障的通透性,可能会使大脑暴露于可能刺激积极免疫反应的毒素或感染,从而释放出新的斑块和缠结的种子蛋白。
莫斯科尼说,与 40 多岁和 50 多岁的女性大脑相比,同一年龄段的男性大脑没有发现明显老化,而且 β-淀粉样蛋白斑块也较少。一种解释是睾酮和雌激素一样,具有神经保护作用——而且男性更年期睾酮水平的下降幅度或速度永远不会像女性更年期雌激素水平的下降幅度或速度那样大。这种差异可能有助于解释为什么患这种疾病的男性较少。莫斯科尼解释说,阿尔茨海默病病理学也可能在女性身上比男性身上更早发展,但女性的补偿能力非常好,以至于她们通常直到疾病发展到晚期才被诊断出来。2019 年的一项研究发现,PET 扫描显示阿尔茨海默病生物标志物的女性在言语记忆测试中的表现优于男性。如果临界值分数是性别特异性的,那么这种疾病可能会在早期被发现,那时干预措施会更有效。
为了进一步识别高危女性,研究人员已开始调查阿尔茨海默病与终生雌激素暴露之间的联系。科学家们用“生殖期”来衡量雌激素暴露,即女性第一次月经来潮和最后一次月经来潮之间的时间跨度。凯撒医疗机构的一项针对 15,754 名会员的大规模研究发现,生殖期为 21 至 34 年的女性患痴呆症的几率比生殖期为 39 至 44 年的女性高 26%,这表明月经初潮晚或更年期早会带来更高的风险。然而,许多因素会影响女性的终生雌激素暴露,但它们的影响尚未得到充分研究。例如,女性怀孕期间的循环雌激素会显著升高,但在分娩后会下降,并且在几年内,仍保持在低于从未怀孕女性的水平。但是,旨在将女性分娩次数与阿尔茨海默病风险联系起来的研究得出了相互矛盾的结果。全世界有超过 1 亿女性服用避孕药,这种药会抑制卵巢激素,但令人震惊的是,人们对避孕药对痴呆症风险的长期影响知之甚少。
激素疗法困境
索菲从青春期开始服用避孕药,并且从未生育过。她说,她的记忆力衰退在围绝经期的最后一年达到了顶峰。她经常每小时经历三次以上的潮热——这种频率和严重程度与大脑中葡萄糖代谢失调加剧、白质流失增多以及日后可能增加痴呆症风险有关。索菲的医生给她开了一种新药:雌激素-孕激素复合片(孕激素保护子宫)。索菲说,效果“非常神奇”:她的潮热消失了,突然间她又记起了早餐会议。
似乎每个更年期女性都应该仅仅为了大脑健康而接受激素疗法,但现实情况更加微妙。在 2000 年代初期,美国国家心肺血液研究所报告了其大规模妇女健康倡议研究及其辅助记忆研究的结果,结果表明,激素疗法(通常是雌激素加孕激素)与乳腺癌、中风、心脏病和血栓的风险增加有关,并且——令人震惊地违背了所有预期——痴呆症的发生率高出两倍。调查人员后来发现了这项研究中的缺陷。女性服用的是结合雌马雌激素,一种半合成形式,人们认为它的神经保护作用不如当今常用的 17β-雌二醇。但更大的问题是,这些女性在开始激素疗法时已经 65 岁或更老了。
女性服用第一片激素疗法药丸(或使用第一支乳膏、阴道环或贴片)的年龄是布林顿所说的“雌激素作用的健康细胞偏倚”的核心。如果神经元是健康的,它们就会对雌激素产生反应。如果神经元老化或长期缺乏雌激素,它们就会对激素变得无反应,因为信号通路会退化,受体会变得功能失调。在这种情况下,添加雌激素甚至可能会加剧神经退行性变。因此,为了使激素疗法发挥好的作用而不是造成伤害,它必须在所谓的关键窗口期内开始,通常是在最后一次月经来潮后的五年内,布林顿说。
几项观察性研究试图在接受激素疗法至少 10 年的患者中检验关键窗口期假说,它们的结果各不相同,从犹他州一项研究中阿尔茨海默病风险降低 30%(该研究中,治疗在更年期发作后五年内开始)到最近一项芬兰研究中风险增加 9% 至 17%(该研究中,开始治疗的年龄似乎不影响风险)。我们应该相信哪个结果?研究人员不知道。尽管他们认为激素疗法对于许多更年期开始的女性来说是安全有效的,但在痴呆症保护方面仍然缺乏共识,并且受到多种因素的制约。“需要进行更多的临床试验,”莫斯科尼说,“尤其是针对仍在围绝经期就开始接受激素疗法的女性。”对于围绝经期症状最严重的女性,例如索菲,她们可能无法自然地很好地适应雌激素的流失;对于她们来说,激素疗法可能会预防更年期过渡期间的神经退行性损害。
“我不敢停药,”索菲谈到她的激素疗法时说。她觉得这种疗法把她从记忆力衰退的恶性循环中拯救了出来,否则她就会像她的祖母一样,一位慈爱而意志坚强的女性,却被阿尔茨海默病折磨得神志不清、疑神疑鬼。然而,索菲没有接受过 APOE4 基因检测,因此尚不清楚她是否真的会患上这种疾病——研究也没有证实激素疗法是否确实有助于预防这种疾病。即便如此,她还是敦促我这个 40 多岁的女性:“你应该在需要时尽快开始服用。” 但肯定有更好的方法来预防阿尔茨海默病吧?
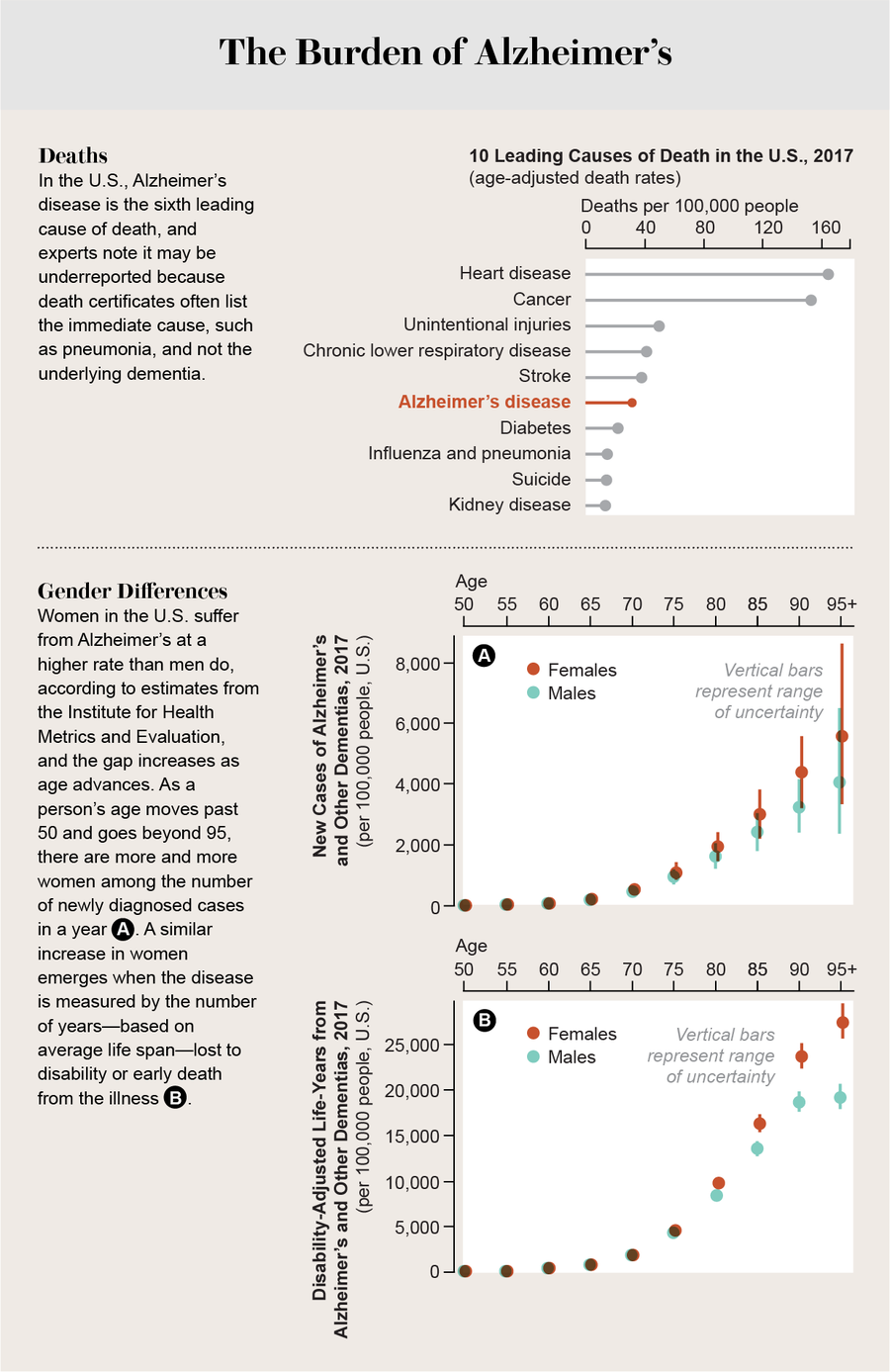
来源:Jen Christiansen;资料来源:“2017 年美国死亡率”,作者 Sherry L. Murphy 等人,《国家健康统计中心数据简报》,第 328 号,2018 年 11 月(主要死亡原因);全球疾病负担合作网络——2017 年全球疾病负担研究 (GBD 2017) 人口与生育率 1950–2017。健康指标与评估研究所,2018 年(性别差异)
脆弱窗口期
更年期不会导致阿尔茨海默病。布林顿说,它更像是一个脆弱窗口期——尤其是对于有潜在风险的女性而言。乍一看,它与阿尔茨海默病之间的联系并不明显。女性更年期的平均年龄为 51 岁;阿尔茨海默病的平均诊断年龄为 70 岁到 75 岁。这中间有 20 多年的差距。但所谓的先兆期——即 β-淀粉样蛋白斑块等初始病理学与全面认知障碍之间——也大约为 20 年。“也许时间只是巧合,”布林顿观察到。“但我不这么认为。”
撇开大脑扫描不谈,是否有可能在女性仍然健康的时候更早地预测她们患阿尔茨海默病的风险?在 2016 年发表的一项研究中,布林顿和她的同事将 500 名健康的绝经后女性分为三组:代谢最佳组、临界高血压组和临界代谢健康组。只有一组在言语记忆测试中的得分显著降低:代谢健康处于临界不健康状态的女性。
从技术上讲,这些受试者的代谢指标仍在正常范围内。然而,有迹象表明她们的健康状况正在朝着错误的方向发展。首先,该组的血糖水平正在接近糖尿病前期阈值,糖尿病前期是一种困扰大约 30% 女性的疾病,本身就与认知障碍有关。饭后,激素胰岛素帮助葡萄糖进入细胞供能,但在患有糖尿病前期的人体内,身体细胞开始对胰岛素产生抵抗力。当脑细胞对胰岛素产生抵抗力时,它们会吸收葡萄糖,但无法对其做出反应——这与更年期葡萄糖代谢减慢相结合,可能会导致神经退行性变。对于许多处于过渡期的女性来说,糖尿病前期是 2 型糖尿病的前奏,后者几乎使阿尔茨海默病风险增加一倍。超过 80% 的阿尔茨海默病患者对胰岛素有抵抗力。
一旦我们将更年期——以及雌激素耗竭——视为改变整个身体的生态,就很容易理解为什么一系列复杂的因素可能会导致阿尔茨海默病,以及为什么管理这些因素是预防的关键。雌激素对心血管系统的健康影响包括胆固醇调节:它可以提高“好”胆固醇 HDL(高密度脂蛋白)胆固醇的水平,并降低“坏”胆固醇 LDL(低密度脂蛋白)胆固醇的水平,后者会导致动脉中形成脂肪性蜡状沉积物。APOE 基因介导胆固醇代谢并将其转运到神经元;e4 基因变异体的携带者血液中的 LDL 胆固醇水平自然较高,并伴有动脉硬化。这些沉积物被炎症松动后,会导致“隐性中风”,使阿尔茨海默病和其他形式的痴呆症风险增加一倍以上。
睡眠也在调节代谢(包括胰岛素敏感性)方面发挥着关键作用,而睡眠不足对女性的影响尤为严重,尤其是在更年期期间。在正常的夜间休息期间,神经胶质细胞会冲洗掉 β-淀粉样蛋白和 tau 蛋白。睡眠剥夺会扰乱这一过程,导致蛋白质积聚并形成斑块,从而导致睡眠片段化,而睡眠片段化会损害葡萄糖代谢,而葡萄糖代谢也会干扰睡眠,如此循环往复,形成加速神经退行性过程的危险循环。同样,APOE4 状态会增加风险:携带者清除或降解斑块和缠结的能力会降低。
压力也会使更年期的临界点提前到来。一项为期 35 年的纵向研究发现,女性在 40 多岁和 50 多岁时经历的持续一个月或更长时间的压力源越多,她们在四十年后患阿尔茨海默病的可能性就越大。与压力一起,女性比男性更可能报告抑郁症,而抑郁症与痴呆症风险几乎翻倍有关。毫不奇怪,女性 APOE4 携带者(她们再次具有最强的阿尔茨海默病遗传风险)比非携带者更容易患上临床抑郁症,这可能是因为大脑中参与情绪调节的区域 β-淀粉样蛋白斑块数量增加。
机会窗口期
在 2019 年,布林顿和她的同事发表了他们对代谢指标研究的后续研究,这次以 APOE 状态作为一个新的变量。携带单拷贝 APOE4 基因的人(约占美国总人口的 25%)比其他人更有可能患上阿尔茨海默病,约占所有病例的 40%。女性患这种疾病的时间比男性携带者早得多,在 65 岁到 75 岁之间,这可能是因为雌激素的神经保护作用丧失。与非携带者相比,携带者的 LDL 胆固醇更高,β-淀粉样蛋白斑块和 tau 蛋白缠结更多,海马体积减少,大脑连接性下降幅度更大。在更年期大脑葡萄糖代谢下降期间,e4 等位基因的女性携带者可能更依赖大脑的酮体作为辅助燃料。
与布林顿之前的研究一样,代谢健康状况不良组在某些认知测试中的得分较低。但这次分析显示,APOE4 携带者是该组表现不佳的主要驱动因素。在携带者中,高胆固醇和其他代谢健康不良的影响加剧了 APOE4 的负面影响,导致早期认知能力下降。然而,当表现不佳组中的携带者接受激素疗法时,她们的代谢健康状况得到了改善,某些认知测试的得分也随之提高。
但布林顿将 APOE4 状态视为“警钟,而不是死刑判决”:许多携带 APOE4 的女性并没有患上这种疾病。在她的研究中,代谢健康最佳组(在认知测试中得分最高)包括阿尔茨海默病基因携带者。这些女性以及健康的非携带者是否更擅长补偿更年期的“生物能量危机”?她们的健康状况是否抵消了其他风险因素?
据 2017 年《柳叶刀》杂志上经常被引用的一份报告称,至少三分之一的阿尔茨海默病病例与糖尿病、肥胖、不良饮食以及其他可预防和可治疗的因素有关。“最重要的信息是,维持代谢健康就能维持认知健康,”布林顿总结道。“你无法改变你的染色体性别或年龄或你的基因变异体。但你可以改变你的代谢健康,从而改变你的风险水平。” 莫斯科尼对此表示赞同。她说,每个人,尤其是 40 多岁和 50 多岁的女性,都应该“了解自己的数字”,意思是 APOE 状态、代谢概况、血液生化指标——甚至大脑扫描图,尤其是在新的性别特异性影像生物标志物出现时。“我希望扫描图能够成为所有中年女性(和男性)临床检查的一部分,以达到预防目的,就像我们检查乳房和子宫一样,”她说。口头禅是“预防”,这个词曾经很少与阿尔茨海默病联系在一起。
激素疗法是否应成为方案的一部分仍然存在争议。但布林顿说,精准医学——利用基因检测和数据分析——正在进入激素疗法领域:医生可能很快就会根据风险生物标志物(如 APOE 状态、生殖史、更年期症状和其他因素)开出精准疗法。并且新版本的激素疗法正在研发中。威斯康星大学密尔沃基分校的神经科学家卡琳·弗里克和她的合作者开发了一种“简化版”17β-雌二醇,据认为它可以降低与标准激素疗法相关的乳腺癌风险。该药物尚未进行临床试验,但在小鼠的初步研究中显示出希望。“它起到了记忆增强剂的作用,”弗里克说。
对于无法预防的阿尔茨海默病病例,布林顿的实验室正在开发一种名为 Allo 的疗法,该疗法基于别孕烷醇酮,一种天然存在的类固醇,可刺激新神经元的产生。在阿尔茨海默病小鼠模型中,Allo 逆转了认知缺陷,恢复了学习和记忆能力。在一项有希望的 1 期临床试验中,轻度痴呆症患者的海马体中再生了灰质体积,脑部炎症也有所减轻。布林顿说,由美国国家衰老研究所资助的针对 APOE4 携带者的 2 期临床试验计划于 2020 年晚些时候开始。
2016 年,美国国立卫生研究院开始要求其资助的研究将性别视为一个生物学变量。阿尔茨海默病的缓慢病程意味着,女性要从更年期过渡的新研究中受益还需要数年时间。与此同时,预防仍然至关重要:建议包括以植物为中心的饮食,这种饮食要低糖、低反式脂肪和饱和脂肪,体育锻炼,减轻压力以及每晚七小时的 β- 和 tau 蛋白清除睡眠,特别是对于中年女性。“女性照顾他人;我们把自己放在最后,”布林顿说。“但我们不能一直拖延健康。”

