美国食品药品监督管理局(FDA)周五批准了一种新药,以减少与镰状细胞病这种罕见血液疾病相关的并发症。
该药物 Endari 由私人控股公司 Emmaus Medical 生产,是近 20 年来首个获得 FDA 批准的镰状细胞病新疗法。然而,Endari 中的活性成分 L-谷氨酰胺是一种可以在柜台购买的旧化学物质,这可能会使 Emmaus 难以获得保险覆盖。
在 Emmaus 的关键临床试验中,与安慰剂相比,使用 Endari 治疗 48 周可减少因镰状细胞疼痛危机而住院就诊的频率和时长。该药物常见报告的副作用包括便秘、恶心和头痛。
支持科学新闻
如果您喜欢这篇文章,请考虑通过以下方式支持我们屡获殊荣的新闻报道 订阅。通过购买订阅,您正在帮助确保有关当今塑造我们世界的发现和想法的具有影响力的故事的未来。
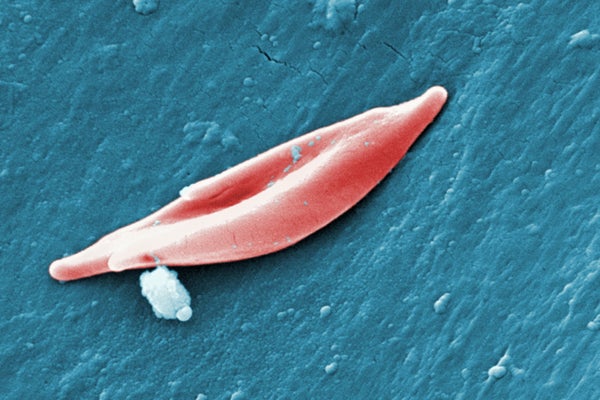
镰状细胞病是一种罕见的遗传性疾病,其特征是红细胞呈异常镰刀状。这些畸形的红细胞会堵塞血管,切断身体组织的氧气供应,导致剧烈疼痛和器官损伤。
根据美国国立卫生研究院的数据,美国约有 10 万人患有镰状细胞病。
虽然 Endari 专注于减少镰状细胞病的并发症,但 Bluebird Bio 正在开发一种基因疗法来治疗该疾病的根本原因并可能治愈患者。使用 CRISPR 基因编辑技术的研究旨在实现相同的目标。
其他致力于开发针对镰状细胞病的新型药物的公司包括 Global Blood Therapeutics 和 Novartis。