卡特琳每天有六次会暂停手头的工作,从口袋里拿出一小块磁铁,触摸到她锁骨下方一块凸起的皮肤。60秒内,她会感到喉咙里传来轻微的震动。如果她说话,声音会颤抖。然后,这种感觉就会消退。
磁铁启动了一个植入式设备,该设备会发出一系列电脉冲——每个脉冲约一毫安,类似于典型助听器所消耗的电流。这些脉冲刺激了她的迷走神经,这是一束从脑干向下延伸到几个主要器官(包括心脏和肠道)的纤维。
迷走神经刺激技术自 1990 年代以来一直用于治疗癫痫,自 2000 年代初以来一直用于治疗抑郁症。但卡特琳是一位 70 岁的阿姆斯特丹健身教练(她要求在此报道中使用化名),她用它来控制类风湿性关节炎,这是一种自身免疫性疾病,会导致关节周围和其他组织中的软骨破坏。她五年前参加的一项临床试验是同类试验中的首例人体试验,它代表了二十年来研究神经系统和免疫系统之间联系的成果。
支持科学新闻报道
如果您喜欢这篇文章,请考虑通过以下方式支持我们屡获殊荣的新闻报道: 订阅。通过购买订阅,您正在帮助确保有关塑造我们当今世界的发现和想法的具有影响力的故事的未来。
对于纽约州曼哈塞特范斯坦医学研究所的神经外科医生凯文·特雷西来说,迷走神经是这种联系的主要组成部分,他说电刺激可能代表治疗自身免疫性疾病(如狼疮、克罗恩病等)的更好方法。
几家制药公司正在投资“生物电子药物”——可以调节神经的设备——以治疗心血管和代谢疾病。但如果特雷西用这种设备控制炎症的目标取得成功,那将是一个重大的飞跃。
肯特州立大学的神经科学家黛安·洛顿说,他是一位先驱,“他让很多人加入进来并在这个领域进行研究”,她花了 30 年时间研究渗透到淋巴结和脾脏等免疫器官的神经。但她和其他观察家警告说,抗炎作用的神经回路尚未得到充分理解。
特雷西承认这种批评,但仍然看到了电刺激的巨大潜力。“在我们有生之年,我们将看到设备取代某些药物,”他说。他认为,对迷走神经或其他周围神经进行电击可以治疗从糖尿病到高血压和出血等多种疾病。“这是一个领域的开始。”
电击价值
特雷西最初走上神经免疫学之路纯属偶然。1998 年,他正在研究一种实验性药物 CNI-1493,该药物通过降低一种名为肿瘤坏死因子-α (TNF-α) 的强效免疫蛋白水平来抑制动物的炎症。CNI-1493 通常通过血液给药,但有一天,特雷西决定将其注射到大鼠的大脑中。他想看看它是否会降低中风期间大脑中的 TNF-α 水平。但发生的事情让他感到惊讶。
大脑中的 CNI-1493 降低了动物全身 TNF-α 的产生。其他实验表明,与直接注射到血液中相比,它的效力高出约 100,000 倍1。特雷西推测该药物作用于神经信号。
他的后续实验支持了这一观点。在将 CNI-1493 注射到大脑几分钟后,特雷西看到一股活动波纹沿着大鼠的迷走神经向下传播2。这条神经高速公路调节一些非自主功能,包括心率、呼吸和将食物推入肠道的肌肉收缩。特雷西认为它也可能控制炎症。当他切断神经并且药物的强大作用消失时,他确信了。“那是一个游戏规则改变者,”特雷西说。这一发现意味着,如果可以刺激迷走神经,甚至不需要药物。
因此,他尝试了一个关键的实验。他给一只大鼠注射了致命剂量的内毒素,内毒素是细菌细胞壁的一种成分,它会使动物陷入炎症、器官衰竭和死亡的恶性循环。该药物的效果大致反映了人类的感染性休克。然后,特雷西使用电极刺激动物的迷走神经。与未治疗的动物相比,接受治疗的大鼠血液中的 TNF-α 含量仅为四分之一,而且它们没有出现休克3。
特雷西立即看到了迷走神经刺激作为阻断 TNF-α 和其他炎症分子激增的一种方式的医疗潜力。公司已经开始销售用于治疗癫痫的植入式刺激器。但是,要将该技术扩展到炎症性疾病,特雷西需要更清楚地说明其工作原理以及可能产生的副作用。
在接下来的 15 年里,特雷西的团队进行了一系列动物实验,以确定迷走神经刺激的作用部位和作用方式。他们尝试在不同位置切断神经4,并使用阻断特定神经递质的药物5。这些实验似乎表明,当迷走神经受到电击时,信号会沿着它向下脉冲到腹部,然后通过第二根神经进入脾脏。
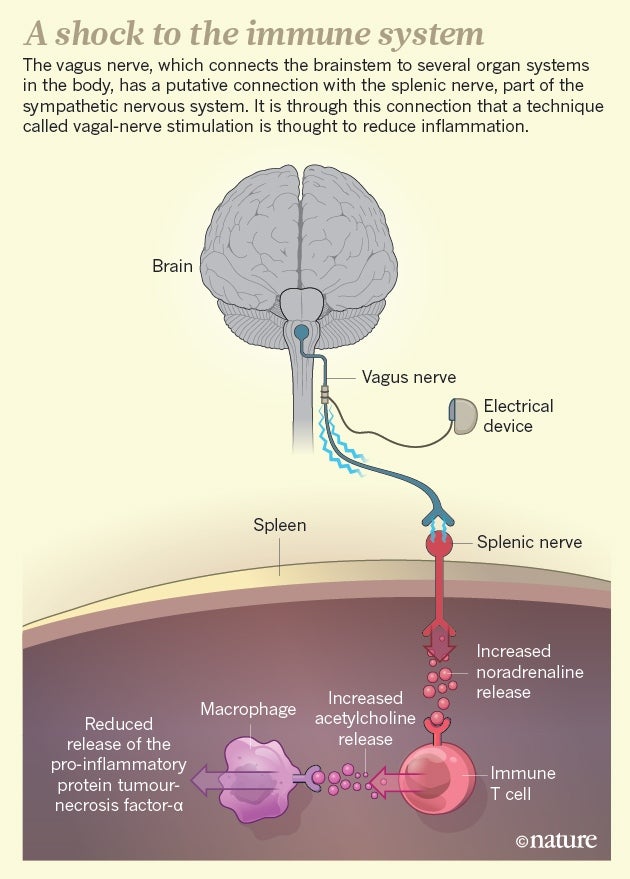
脾脏有点像免疫学的卡车停靠站,循环免疫细胞会在那里定期停留一段时间,然后再返回血液。特雷西的团队发现,进入脾脏的神经会释放一种称为去甲肾上腺素的神经递质6,它直接与脾脏中称为 T 细胞的白细胞进行通信。神经和 T 细胞之间的连接实际上类似于两个神经细胞之间的突触;特雷西说,T 细胞几乎就像神经元一样在发挥作用。当受到刺激时,T 细胞会释放另一种神经递质,称为乙酰胆碱,然后乙酰胆碱与脾脏中的巨噬细胞结合。正是这些免疫细胞通常会在动物接受内毒素时将 TNF-α 喷射到血液中。然而,暴露于乙酰胆碱会阻止巨噬细胞产生炎症蛋白(参见'免疫系统的冲击')。
特雷西的发现为几十年来一直在进行的研究赋予了新的意义。在 1980 年代和 1990 年代,当时在纽约罗切斯特大学担任神经解剖学家的戴维·费尔顿捕捉到了各种动物体内混合神经元-T 细胞突触的显微图像7——不仅在特雷西看到的脾脏中,而且在淋巴结、胸腺和肠道中也发现了。这些神经元属于所谓的交感神经系统,该系统调节身体对某些应激源的反应。正如特雷西在脾脏中发现的那样,费尔顿观察到这些交感神经元通过分泌去甲肾上腺素来刺激其 T 细胞伙伴——而且,这种刺激通常有助于减轻炎症。
2014 年,日本大阪大学的神经免疫学家中井明子报告说,有证据表明交感神经对 T 细胞的刺激会限制它们离开淋巴结并进入循环系统,否则它们可能会在身体其他部位引起炎症8。但在许多自身免疫性疾病中,这种神经信号传导被破坏了。
洛顿和她的双胞胎姐妹、加利福尼亚州洛马琳达大学的神经科学家丹尼斯·贝林格发现,在自身免疫性疾病的大鼠模型中,交感神经通路发生了改变9。人类也观察到同样的情况。交感神经因去甲肾上腺素过度释放而受损,这导致它们从本应调节的免疫细胞中撤出。随着疾病的进展,这些神经又会回到它们放弃的组织中——但它们以异常的方式这样做,并与不同的免疫细胞亚群建立联系。这些重组的神经通路实际上维持了炎症,而不是抑制炎症9。贝林格说,这种情况发生在脾脏、淋巴结和关节等部位,并导致了大量的病理。
但她、洛顿和其他人对特雷西关于迷走神经刺激降低炎症的途径的说法持怀疑态度。澳大利亚墨尔本大学的神经科学家罗宾·麦卡伦一直在寻找迷走神经与刺激脾脏中 T 细胞的神经之间的联系——但到目前为止,他还没有找到。
贝林格说,迷走神经刺激“是通过其他神经间接起作用的”。她说,在转向人体治疗之前,正确绘制这些神经回路图非常重要。“解剖结构对于你可能会看到的副作用类型有很大影响。”
然而,即使是这些怀疑论者也看到了特雷西方法的潜力。贝林格指出,在许多自身免疫性疾病中,不仅交感神经在重组成促炎回路时变得过度活跃,而且与之相对的迷走神经也变得不活跃。迷走神经刺激可能部分恢复这两个神经系统之间的平衡。“这是第一步,”她说。“我相信他们会将其引入临床,并且他们会显示出显著的效果。”
患者方法
接受迷走神经刺激治疗癫痫或抑郁症的人会出现一些副作用——例如喉部疼痛和紧绷,或声音嘶哑;卡特琳在刺激迷走神经时会感到轻微的版本。电击这条神经还会降低心率或增加胃酸等其他影响。
在这方面,特雷西有理由感到乐观。人类的迷走神经包含大约 100,000 根独立的神经纤维,这些纤维分支出来到达各个器官。但是,触发神经活动所需的电量在不同的纤维之间可能会相差 50 倍之多。
特雷西的前研究生雅科夫·莱文已经计算出,参与减少炎症的神经纤维具有较低的激活阈值。只需 250 毫微安(安培的十亿分之一)即可将其打开——这只是通常用于抑制癫痫发作的电量的八分之一。尽管接受癫痫发作治疗的人每天需要长达数小时的刺激,但动物实验表明,单次短暂的电击就可以长时间控制炎症10。莱文说,受到乙酰胆碱冲击的巨噬细胞在长达 24 小时内都无法产生 TNF-α,他现在在曼哈塞特的 SetPoint Medical 公司工作,该公司成立的目的是将迷走神经刺激商业化为一种医疗方法。
到 2011 年,得益于动物研究和莱文的优化努力,SetPoint 准备在人体中尝试该技术。首次试验由阿姆斯特丹大学和英国制药公司葛兰素史克公司的风湿病学家保罗-彼得·塔克监督。在几年时间里,包括卡特琳在内的 18 名类风湿性关节炎患者植入了刺激器。
她和其他 11 名参与者在 6 周的时间内症状有所改善。实验室测试表明,他们血液中炎症分子(如 TNF-α 和白细胞介素-6)的水平降低。当设备关闭 14 天后,这些改善消失了——然后在重新开始刺激后又恢复了。
卡特琳从此以后一直在使用刺激器,她仍然每周注射一次抗风湿药物甲氨蝶呤,以及每天服用一次名为双氯芬酸的抗炎药——但她能够停止服用大剂量免疫抑制类固醇,她的关节也得到了足够的改善,可以重返工作岗位。这项试验的结果于去年 7 月发表在《美国国家科学院院刊》上11。
另一项迷走神经刺激试验的结果也在同一时间左右发表12。法国格勒诺布尔大学医院的胃肠病学家布鲁诺·博纳兹将刺激器植入到七名克罗恩病患者体内。在六个月的时间里,其中五人报告说症状有所减轻,对他们肠道的内窥镜检查显示组织损伤减少。SetPoint 也正在进行一项针对克罗恩病的迷走神经刺激治疗的临床试验,目前已进行到一半。
特雷西和博纳兹并不是唯一希望利用神经回路治疗炎症的人。加利福尼亚大学圣地亚哥分校的创伤外科医生劳尔·科因布拉正在研究它作为治疗感染性休克的方法,感染性休克每年影响数十万人。许多死于这种疾病的人都被一个单一事件推到了不归路:肠道内壁的迅速恶化,这会将细菌释放到体内——从而引发炎症,损害包括肺和肾脏在内的器官。
与特雷西一样,科因布拉也通过刺激迷走神经,无论是通过电刺激13还是通过施用一种名为 CPSI-121 的实验性药物(参考文献14),成功地抵消了动物体内的这种致命序列。科因布拉希望将这项工作带入临床试验。但他的研究也揭示了迷走神经刺激必须克服的另一个主要挑战:与大鼠不同,有些人可能对该技术具有抵抗力。
人类基因组编码了一种在其他动物中未发现的额外的、非功能性乙酰胆碱受体蛋白。科因布拉的合作者托德·科斯坦蒂尼也在加利福尼亚大学圣地亚哥分校,他发现如果这种异常受体产生量足够大,它会破坏信号传导,并使巨噬细胞对乙酰胆碱无反应。即使受到迷走神经刺激,它们也可能继续释放 TNF-α15。科斯坦蒂尼说,人们产生的这种蛋白质的数量范围相差 200 倍。他计划对人们进行测试,以确定高水平是否真的会阻断迷走神经刺激的抗炎作用。轶事证据表明,情况可能确实如此。
迄今为止进行的小型临床试验表明,有些人对迷走神经刺激没有反应。可能是测试可以确定哪些人会从治疗中受益,然后再给他们植入植入物。
然而,尽管存在不确定性,生物电子药物领域正开始获得动力。去年 10 月,美国国立卫生研究院宣布了一项名为“刺激周围活动以缓解疾病 (SPARC)”的计划,该计划将在 2021 年之前提供 2.38 亿美元的资金,以支持研究更新胸腔和腹腔神经回路图。
葛兰素史克公司也表现出兴趣。它已投资 SetPoint,并于去年宣布与谷歌成立一家合资企业——名为 Galvani Bioelectronics——将开发一系列疾病的疗法,包括炎症性疾病。
迷走神经刺激是否能达到预期效果还有待观察。迄今为止接受治疗的人数微乎其微——在 2 项已完成的试验中只有 25 人。而且治疗方法在这些早期试验中通常看起来很有希望,但在规模更大的试验中却会失败。
但自身免疫性疾病患者开始注意到这一点。类风湿性关节炎和克罗恩病的治疗存在一定的风险,并且并非对所有人都有帮助。卡特琳是 1000 多名咨询迷走神经刺激试验的人之一。“我别无选择,”她说。“我想要它。”
编者注:本文的早期版本错误地暗示凯文·特雷西发起了首个人体类风湿性关节炎迷走神经刺激试验。实际上是 SetPoint Medical,一家他共同创立的公司。此外,主持该试验的保罗-彼得·塔克于 2011 年加入葛兰素史克公司,而不是 2016 年。
本文经许可转载,并于2017 年 5 月 3 日首次发布。