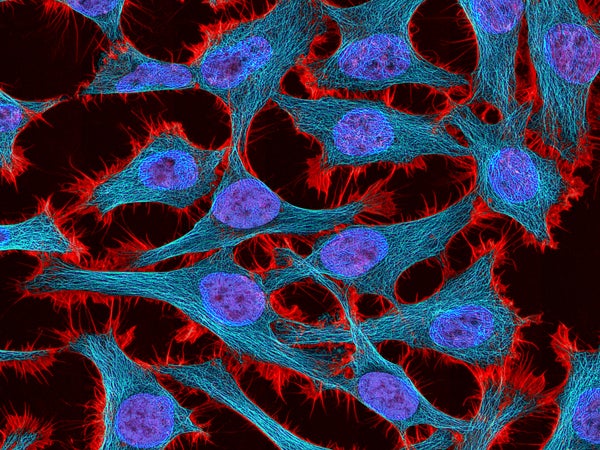
科学家们长期以来都熟悉汉丽埃塔·拉克斯的细胞——但围绕这些细胞的伦理争议使她在更广阔的世界中声名鹊起。
她的声名鹊起归功于 2010 年出版的获奖书籍,该书探讨了在拉克斯接受癌症治疗的过程中,医生如何分离出后来成为首批“永生”人体细胞的细胞。海拉细胞在她体外存活、繁衍和增殖,以至于 65 年来一直在世界各地的实验室中持续使用,尽管拉克斯本人已于 1951 年死于癌症。但它们的使用引发了关于未经同意采集的医疗样本以及个人及其家人应如何因基于其组织的发现而获得补偿的具有挑战性的问题。
现在,这个故事将成为本月晚些时候上映的HBO 电影的主题,这使其成为反思汉丽埃塔·拉克斯是谁以及她的细胞为科学做出了哪些贡献的绝佳时机。以下仅是其中一部分。
关于支持科学新闻报道
如果您喜欢这篇文章,请考虑通过以下方式支持我们屡获殊荣的新闻报道 订阅。通过购买订阅,您正在帮助确保有关塑造我们当今世界的发现和想法的具有影响力的故事的未来。
为女孩接种癌症疫苗
在 20 世纪 80 年代初期,德国病毒学家哈拉尔德·楚尔·豪森发现海拉细胞包含多人乳头瘤病毒 18 型 (HPV-18) 的多个拷贝,HPV-18 是后来发现会导致拉克斯死于宫颈癌的 HPV 毒株之一。HPV-18 被认为是该病毒最危险的毒株之一,它将其 DNA 插入正常细胞并迫使它们产生最终导致癌症的蛋白质。在拉克斯的案例中,病毒进入细胞并关闭了通常会抑制肿瘤形成的基因。多年后,科学家们利用这些知识开发了 HPV 疫苗,这些疫苗现在已广泛使用,并被认为使少女 HPV 感染病例减少了近三分之二。哈拉尔德·楚尔·豪森因其发现而获得了 2008 年诺贝尔奖。
向我们展示细胞如何保持年轻
由于拉克斯细胞看似无限的寿命,我们现在更好地了解了一些细胞如何在时间流逝的情况下保持“年轻”。通常,当细胞分裂时——无论是随着人的成长还是身体修复损伤——每次分裂都会切掉染色体末端,称为端粒。随着时间的推移,这意味着染色体会变得稍短,这被认为是细胞衰老的驱动因素。
在 20 世纪 80 年代,人们发现一些动物胚胎具有一种称为端粒酶的酶,它可以保护染色体免于降解,使细胞能够保持活跃分裂。然后在 1989 年,耶鲁大学科学家格雷格·莫林使用海拉细胞首次在人体细胞中分离出相同的酶。莫林假设这种在癌细胞中发现的酶也是胚胎细胞如何在生命之初快速分裂的原因。在 1996 年,当科学家在人体胚胎中发现端粒酶时,他的假设被证明是正确的——这就是使它们能够快速生长直到出生,而人体在出生后就停止制造它的原因。
根除脊髓灰质炎
在拉克斯去世时,脊髓灰质炎是世界上最具破坏性的病毒性疾病之一。海拉细胞帮助疫苗更快地上市。在 20 世纪 50 年代初期,乔纳斯·索尔克已经弄清楚了疫苗的工作原理;问题是如何测试它。通常,索尔克会在猴子的细胞上测试疫苗。但猴子及其细胞很昂贵,特别是考虑到测试疫苗实际上会杀死细胞。理想情况下,用于测试的最佳细胞应该容易感染脊髓灰质炎病毒,但不会被其杀死。在研究人员发现海拉细胞之前,不存在这样的细胞。这些细胞不仅比科学家以前使用的细胞更容易感染病毒,而且快速生长的细胞几乎不可能杀死。塔斯基吉大学的科学家们建造了一家工厂来复制海拉细胞,使索尔克能够成功地测试疫苗,该疫苗在过去 60 年中有效地消除了世界上大多数国家的脊髓灰质炎。
绘制人类基因组图谱
在 20 世纪 60 年代中期,海拉细胞与小鼠细胞融合,创造了第一个有记录的人-动物杂交细胞。反过来,这些细胞在基因绘图的早期变得非常重要。由于每个杂交体都会有不同的人和小鼠基因组合,科学家可以观察细胞产生或不产生哪些蛋白质,并推断出它们是由哪些人类基因产生的。随着时间的推移,这些技术演变成了人类基因组计划产生的精细人类基因组图谱。
欧洲科学家后来发表了拉克斯的基因组,但在她的家人抗议后将其从公众视野中移除。2013 年,美国国立卫生研究院和拉克斯的后代发布了一套处理拉克斯基因组的特殊规则。
开创病毒学领域
多年来,科学家们用各种病毒——艾滋病病毒、疱疹病毒、寨卡病毒、麻疹病毒和腮腺炎病毒等——感染了顽强的海拉细胞,以更好地了解如何对抗它们。例如,他们发现一种称为 T 细胞的白细胞表面有一种称为 CD4 的表面蛋白,艾滋病病毒就是利用它进入细胞的。当将 CD4 添加到海拉细胞中时,它们可能会感染艾滋病病毒,从而可以在海拉细胞上测试艾滋病病毒药物。
研究人员还了解到,麻疹病毒在感染海拉细胞时会不断变异,使该疾病更难对抗。最近,微生物学家发现寨卡病毒无法在海拉细胞中繁殖。深入研究其原因可能会产生针对该疾病的新疗法或疫苗。